CROで働く魅力とは
魅力1 成長業界
世界の医薬品開発に欠かせないCRO。日本でも今後の成長が見込まれています。
“臨床試験のプロフェッショナル”として、医薬品の開発を支援するCRO。その市場規模は、この16年で急速に拡大しています。とりわけ国内市場では2000年以降、売上高にして10倍以上の成長をとげています。日本で初めてCROが登場したのは1980年代のことですが、その後の認知度拡大や、関連する法規定の整備もあり、今では医薬品開発に欠かせない存在となっています。
日本CRO協会会員企業の売上高と従業員数の推移
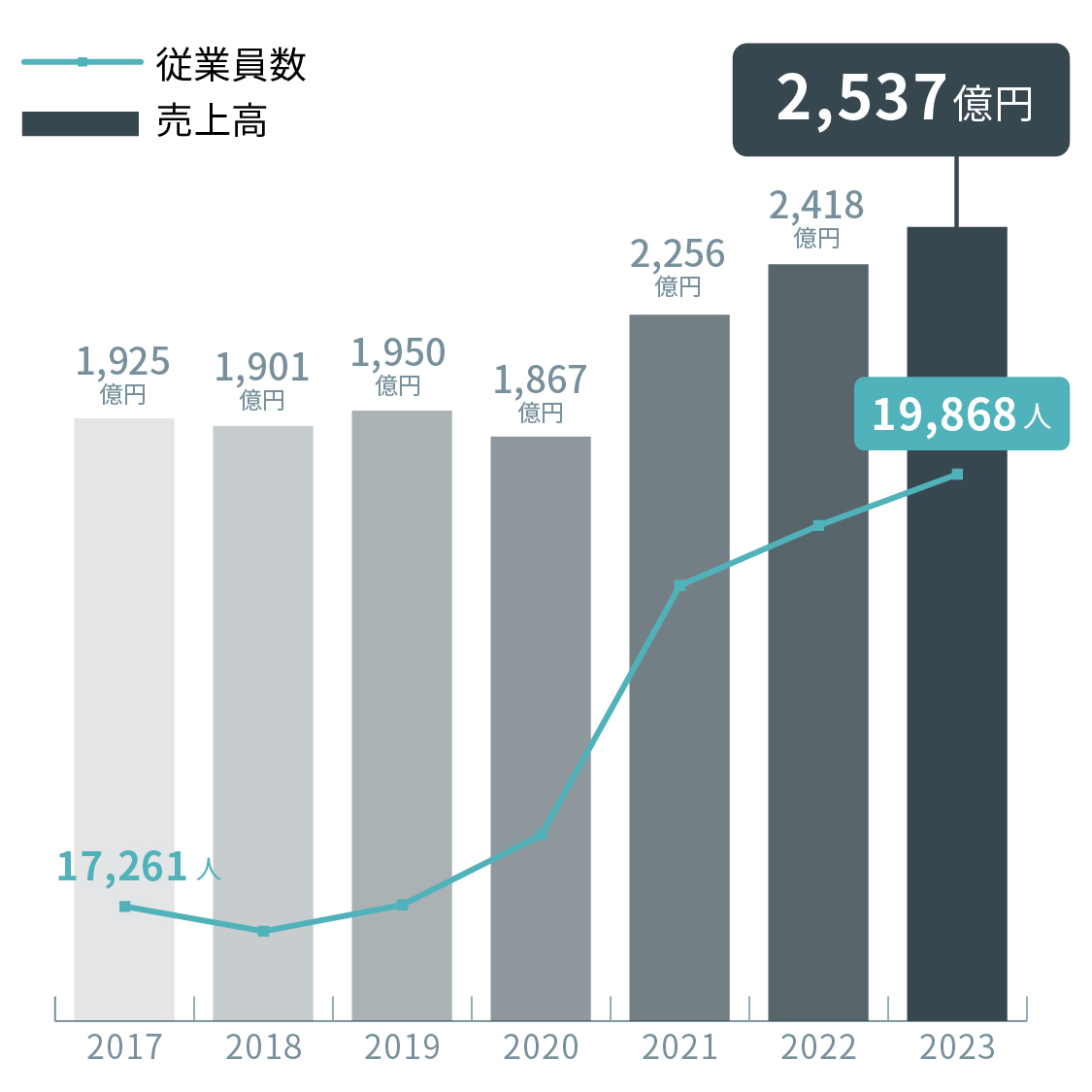
魅力2 高い社会貢献性
新しい医薬品を、安全に、効率よく生み出すための業務を支援し、人々の健やかな暮らしに貢献しています。
新たな医薬品の安全性・有効性を科学的に検証するために、被験者への影響を調べるのが「臨床試験(治験)」です。臨床試験では厳格に定められたルールに則り多くの段階を経る必要があり、すべてを終えるまでには膨大な時間と費用がかかります。法的手続きなども段階ごとに発生するため、多くの開発品目を抱える製薬会社にとって、大きな負担となっています。
CROは、こうしたさまざまな業務を製薬会社に代わって行うことで、医薬品の安全・安心を支えるとともに、新薬開発のスピードアップにも貢献し、一日でも早く患者さんの元へ届けるサポートをしています。
CROの位置付けと役割
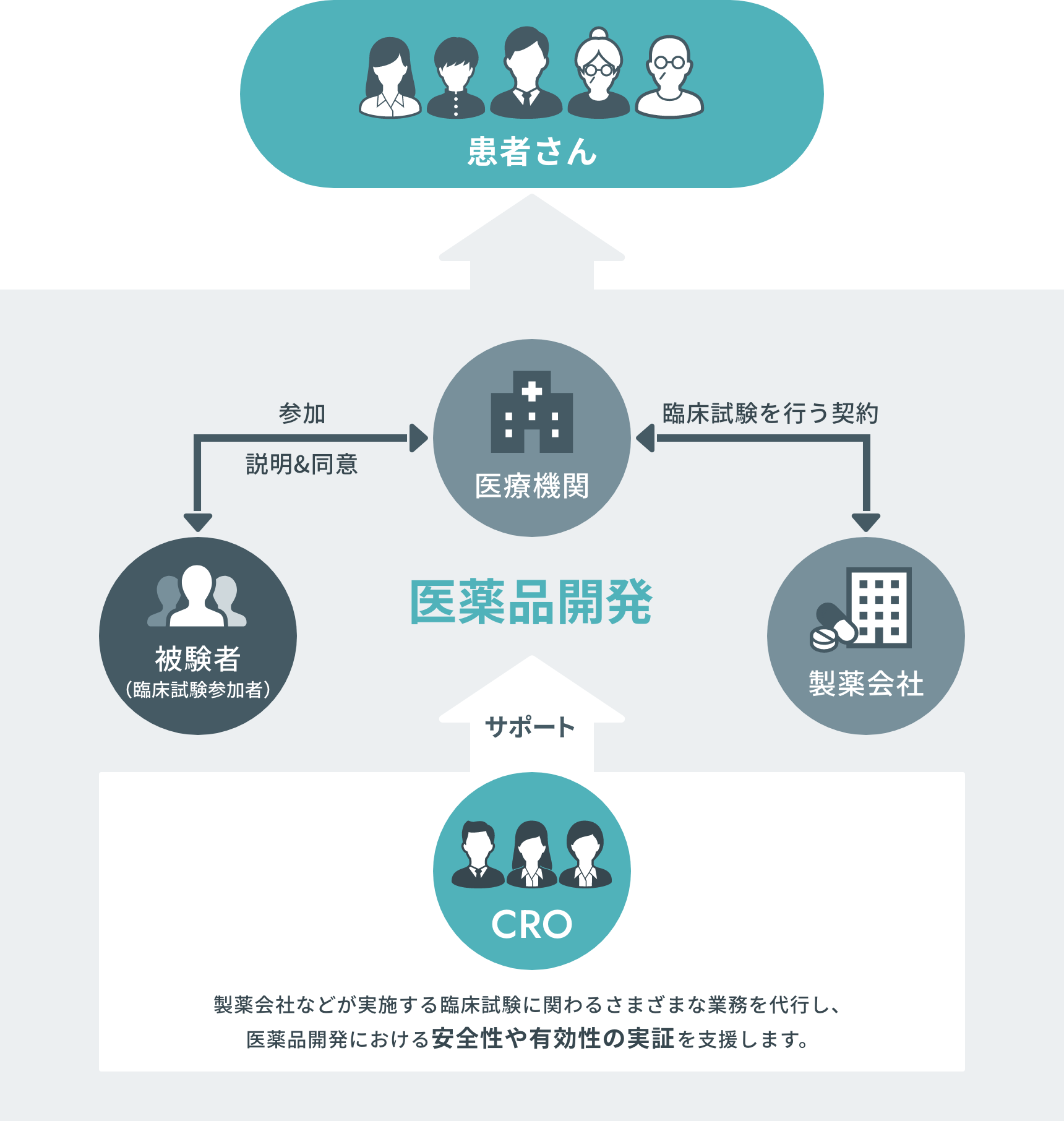
1つの医薬品ができるまで
出典:日本製薬工業協会 てきすとぶっく製薬産業2016-2017 開発費は日本CRO協会による推計
魅力3 医療従事者としての専門性
医薬品の開発現場と医療現場を結ぶ、プロフェッショナルとして働くことができます。
医薬品の安全性・有効性の評価には、何より正確さが求められます。このため臨床試験でも、まずは健常者、次いで少数の患者・・・と対象を変えて繰り返しデータをとり、必要なら投与量や使用法を変えるといった複雑なプロセスが必要となってきます。加えて、医薬品の発売後にも追跡調査(製造販売後調査)を行い、慎重に影響を見定めることとなります。
こうした中、データの収集・資料化から関係機関への連絡、必要な法的手続きの支援までを一手に担い、すべてのプロセスをスムーズに進行するのがCROです。多くの知識やノウハウを必要とする、まさに“プロフェッショナルの仕事”といえます。
 |
新薬となる可能性のある新規物質の創製や候補物質の選別を行います。 |
 |
主に動物を使って科学的に候補物質を調べ、安全性などを検討します。 |
 |
臨床試験をCROが支援!第Ⅰ相試験 少数の健常者による安全性の確認試験を行います。 第Ⅱ相試験 少数の患者で安全性と有効性を確認します。投与量、使用法などを設定します。 第Ⅲ相試験 多数の患者で既存薬またはプラセボ(偽薬)と比較して、新薬の有効性と安全性を検証します。 |
 |
承認申請をCROが支援!臨床試験で新薬の有効性や安全性が確認された後、行政当局に承認申請します。 |
 |
製造販売後の調査もCROが支援!臨床試験段階ではわからなかった効果や安全性を確認するために、販売された後も、広範囲に調査・分析を行います。 |
魅力4 キャリアの多様性
多様な専門性を身につけ、自分らしい働き方でキャリアアップを目指すことができます。
臨床試験や製造販売後調査において、CROが携わる業務の範囲は多岐にわたり、それぞれの業務で高い専門性が必要となります。このため、さまざまな業務に関わる中で専門性を広げ、成長していくことができます。
また、“人”が資本の仕事であることから、CRO各社は独自の教育・研修制度や福利厚生制度を整備しており、キャリアアップやワークライフバランスへの支援が充実していることも大きな魅力です。
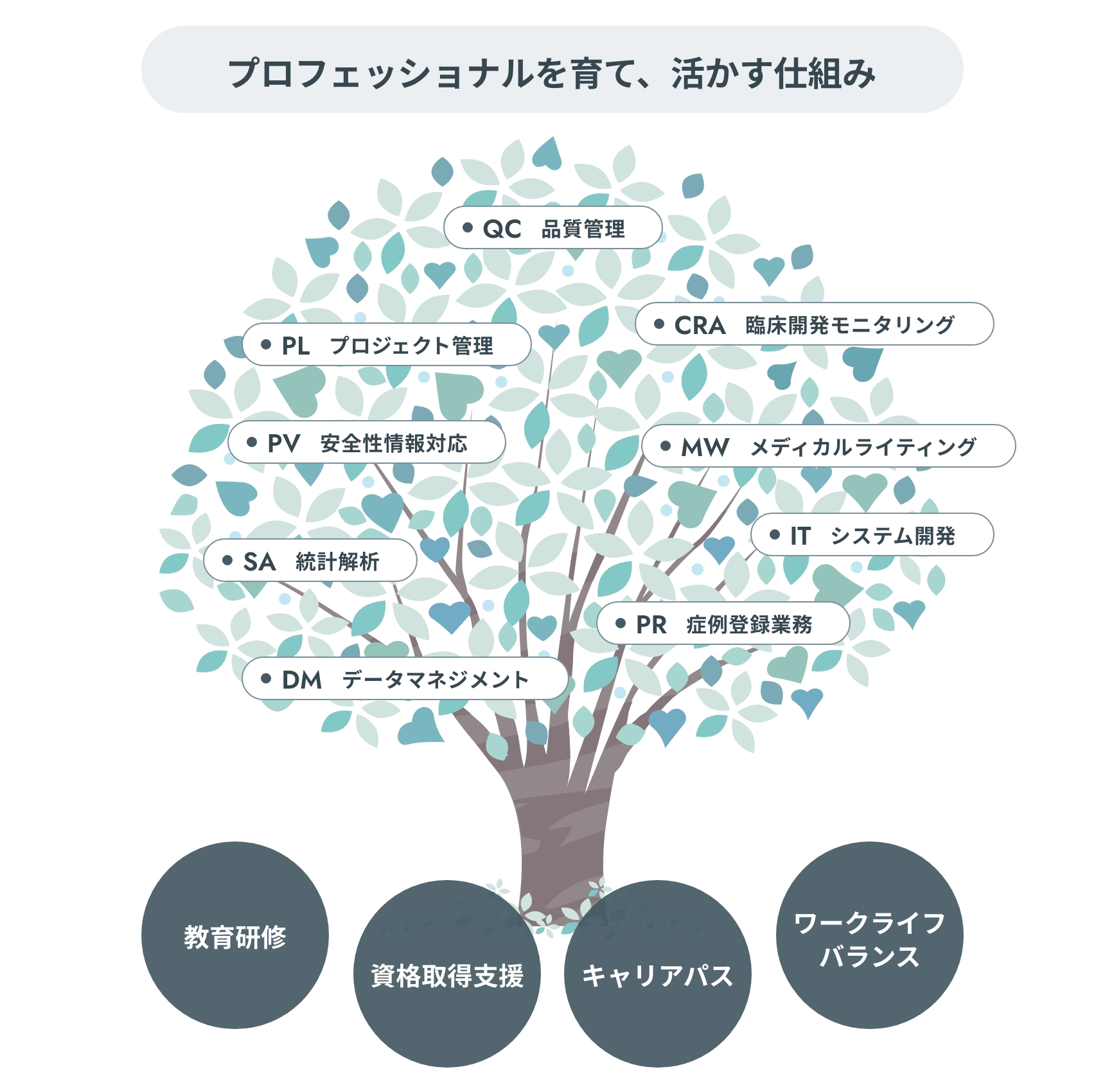
魅力5 広がる可能性
新たな医療や国際共同治験など、活躍の場はますます広がっています。
近年、先端医療の領域では、オーファンドラッグ※の開発や、iPS細胞技術に基づく再生医療など、新たな分野での研究が盛んに進められています。こうした動きに伴い、CROが担うべき役割はこれまで以上に多彩なものとなっています。
また、国際ルールの整備を背景に、海外企業による日本国内での臨床試験、国を越えた共同治験などの機会も増加しています。今後もCROの活躍の場はますます拡大していくと見られます。
※患者の絶対数が少ないなどの理由から、これまで十分な研究が進んでこなかった疾患に対応する医薬品
新しい領域
外資系製薬会社からの委託が大幅に増加

出典:日本CRO協会 年次報告書(2003,2015)






